3. mRNA製劑與冷鏈保存
一. mRNA脂質納米顆粒(LNP)製劑
RNA原液製成後的另一個挑戰便是RNA的遞送系統,RNA疫苗與蛋白質疫苗的不不同點是RNA比較不穩定,且mRNA除了打入人體且必需送入細胞內,並透過人體細胞生產蛋白質才有作用,整個過程必需安全運送mRNA至細胞內,mRNA疫苗才有作用,而蛋白質疫苗則只要打入人體即可,因此遞送系統的建立是mRNA疫苗成功的重點關鍵之一,可以說沒有RNA的遞送系統,就沒有mRNA疫苗的問世。目前各家建立的遞送系統略有不同,但主要的成分如下:
陽離子脂質:在形成LNP時,mRNA帶負電和帶正電的陽離子脂質體在特定酸鹼(pH)值下混合,因靜電吸引會融合在一起幫助形成LNP,在細胞內,因細胞內的pH環境,反而幫助釋放mRNA進入細胞質內。陽離子脂質在協助LNP顆粒的形成與mRNA在細胞內的釋放,是脂質微粒最關鍵成分。以陽離子脂質作為載體有著寬廣的應用前景,一些陽離子脂質會引起細胞毒性,陽離子脂質的細胞毒性取決於其親水性頭基的結構。
聚乙二醇脂質: 修飾的聚乙二醇脂質體形成親水保護層,維持LNP空間的穩定性,可延長脂質微粒在體內代謝時間,提高LNP穩定性與壽命,聚乙二醇在顆粒表面可遮罩血漿蛋白等成分結合顆粒,以避免LNP顆粒在體內被清除。
膽固醇:膽固醇有助於增加細胞膜的流動性或硬度,可增加LNP結構的穩定性。
合成磷脂:磷脂醯膽鹼,輔助型脂質,可以在內吞作用時加快mRNA的釋放。
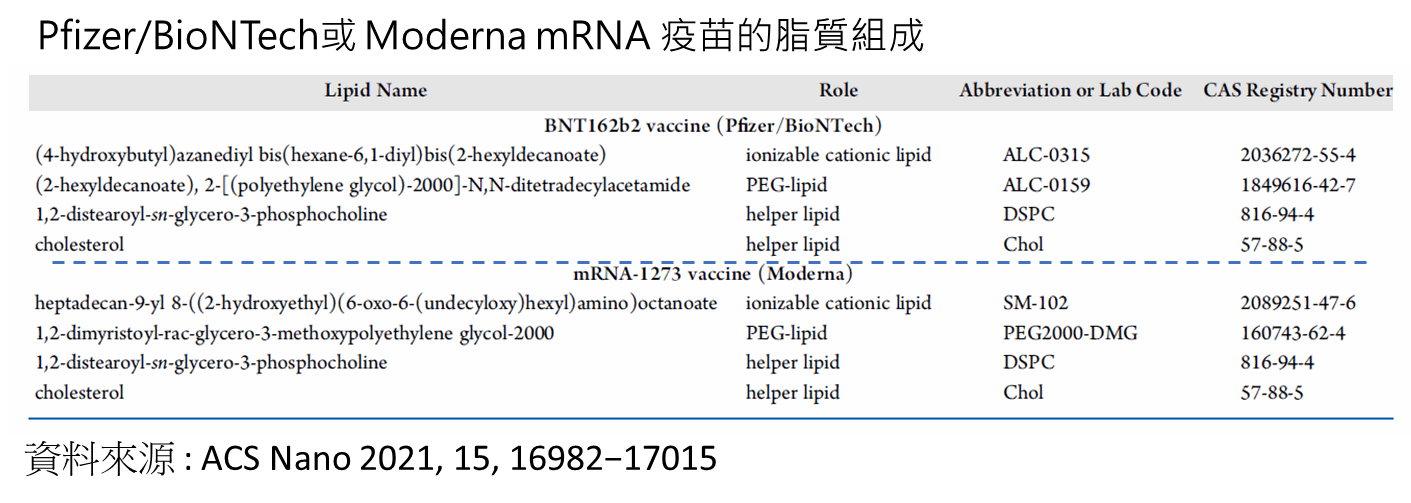
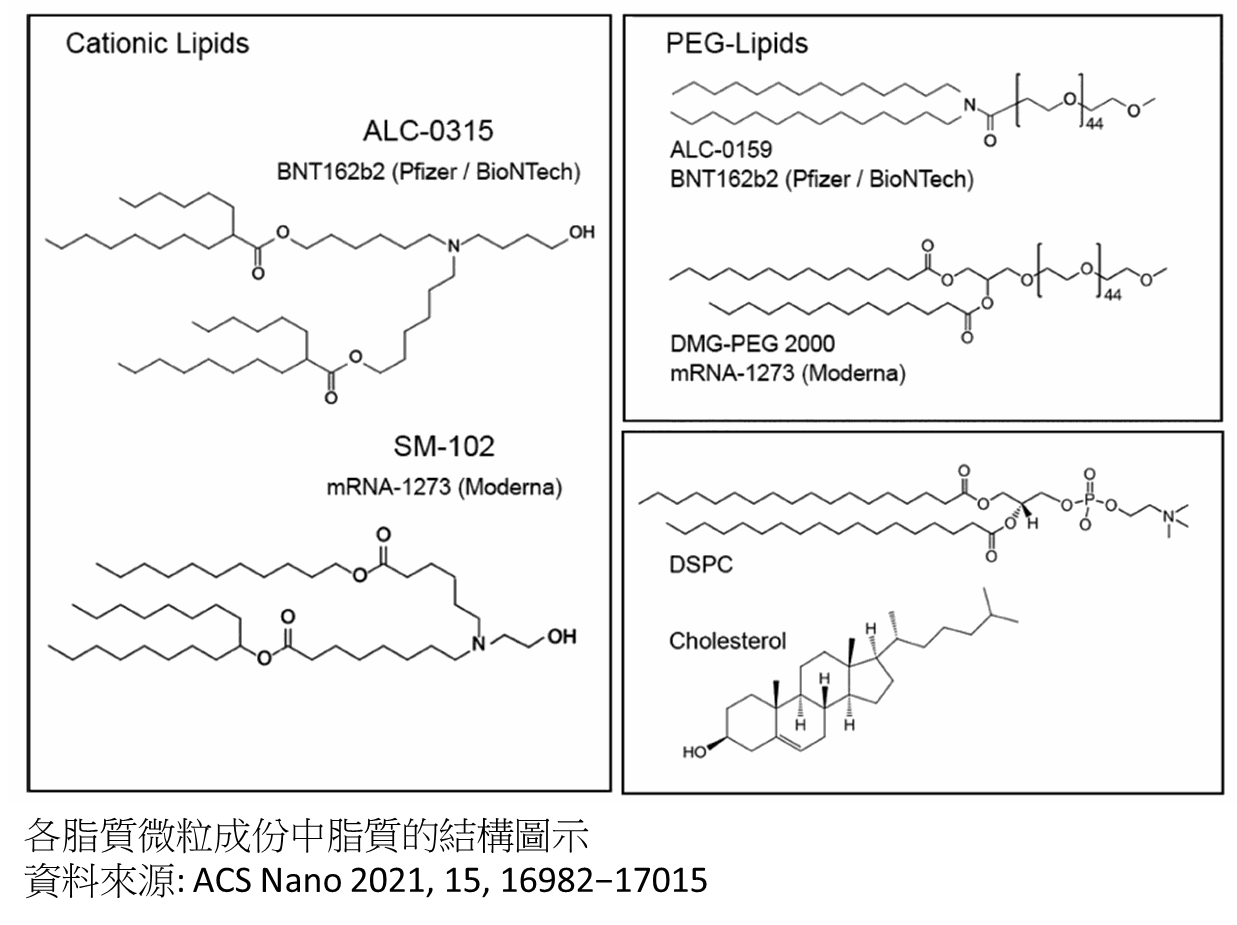
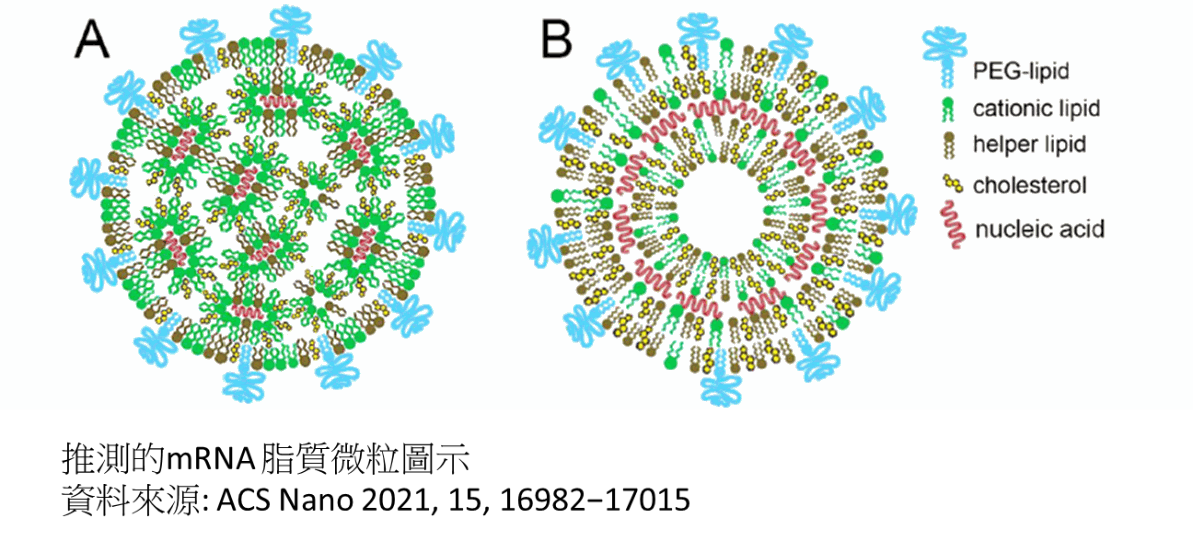
鴻林堂公司已經於2021年10月在新竹科學園區成功合成陽離子脂質ALC-0315,首次合成7公克供驗證效能使用。第二試產為產能放大50倍,將於2022年三月完成350克的陽離子脂質ALC-0315生產。若生產成功,將在2022年五月在新竹科學園區開始試驗批次5公斤的陽離子脂質生產。由於ALC-0315為Pfizer/BNT版本,鴻林堂公司也已在2021年10月實現小量SM-102的陽離子脂質製作,此為Moderna版本所用的材料。
納米顆粒(LNP)製劑的生產也是mRNA疫苗的關鍵工藝步驟。目前工業放大工藝多數採用微流控混合技術來製備LNP,以控制形成的粒徑大小,此法係將脂質與核酸分別溶解在有機相與水相後,將兩相溶液經由不同的通道進入微流控制製備系統,並透過適合大小的孔徑出口,由改變流體注入速度和比率,就可以控制脂質納米顆粒的粒徑大小與分佈,目前文獻上指出,約在100 nm粒徑的效果較佳。
此LNP的品質控管重點有:複合率和/或包覆率、包覆前mRNA溶液的pH值,包覆後pH值,平均粒徑及粒徑分佈、粒子微觀形態,Zeta電位、滲漏/釋放數值等分 析。
二. 冷鏈保存
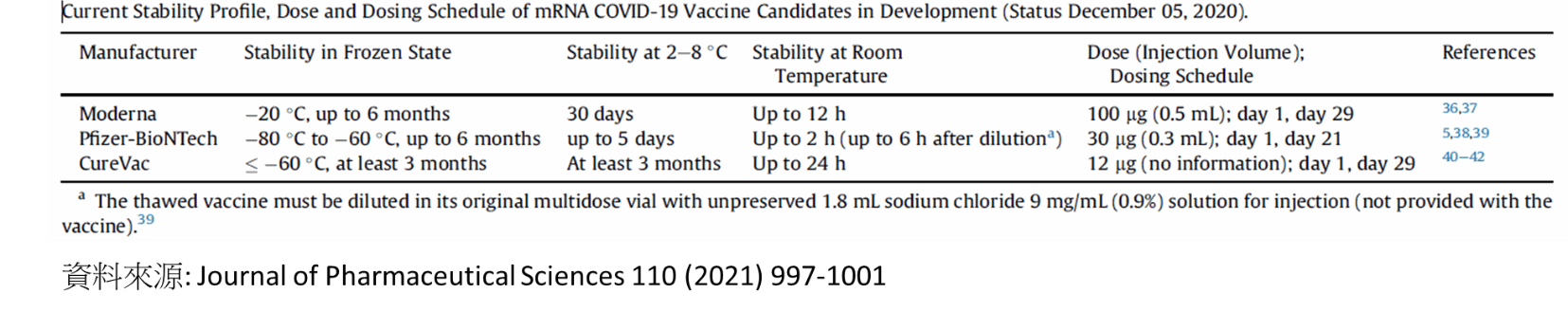
因為mRNA對溫度非常敏感,其保存時間隨著溫度的提升而下降,也是目mRNA疫苗保存甚至運送時的痛點,目前的運送與保存溫度皆需超低溫度保存,下 表 為目前各家mRNA疫苗的保存及運送條件.