1.DNA原液
一. 質體設計與構築
可誘發抗體的物質稱為抗原,可當作抗原的物質有很多種,其中最常見的是蛋白質,傳統的疫苗或用減毒的病毒(菌),或去活化的病原體製成疫苗,這種方式生產的技術門檻較低,可快速製成疫苗,但因為是採用整個病原體,故需要承受的風檢較高,近來因分子生物技術的發展與蛋白純化技術的進步,則開始有蛋白質製成的疫苗、DNA製成的疫苗、mRNA製成的疫苗。以目前新冠病毒疫情而言,BNT/Pfizer、Moderna等公司以mRNA疫苗證實其產生的抗體與T細胞免疫可有效防止病毒感染或預防重症等重大成果,在 mRNA疫苗的開發中,第一步是先設計用來表現RNA的DNA質體,此時需先決定選用病毒(菌)的那一種或那些蛋白為主要的抗原,以新冠病毒為例,學理上新冠病毒的棘蛋白(spike protein)是病毒感染與進入人體細胞的關鍵蛋白,故選擇棘蛋白當作抗原,則以它所產生的抗體或T細胞免疫,可專一性中和(或結合)病毒的棘蛋白,使病毒在入侵細胞前就被免疫系統辨識及排除,因此BNT/Pfizer與Moderna等公司皆是採用棘蛋白作為抗原。
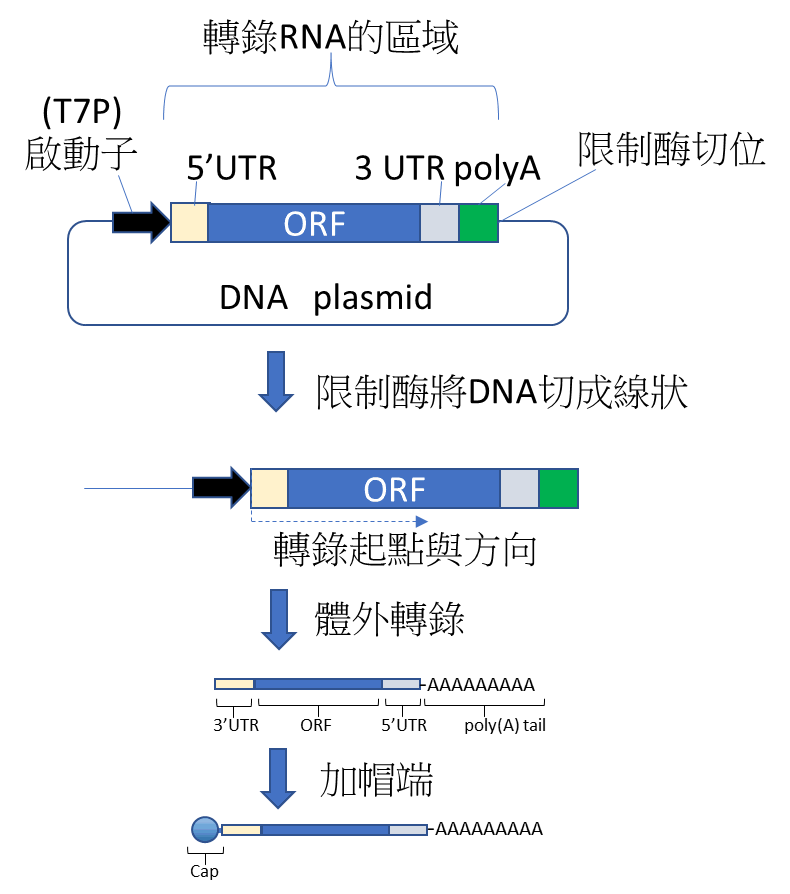
採用mRNA的技術需先了解mRNA的結構及其在生物學所扮演的角色。生物體表現蛋白的方式為DNA先產生(轉錄)RNA,而RNA再產生(轉譯)出蛋白質,下圖為DNA 質體 設計的圖示,其序列包括對應RNA的5’端非轉譯區(5’UTR)、目標蛋白轉譯區(ORF)、3’端非轉譯區(3’UTR)、聚合體(A)尾(poly(A)tail)皆需要構築在啟動子之後,如T7 啟動子簡稱T7P,並在polyA尾巴之後設計一個限製酶的切位,此切位可用限制酶將質體切成線狀,此線狀DNA可用於之後的體外轉譯反應以生產RNA,RNA則再經修飾加帽端即可形成mRNA。
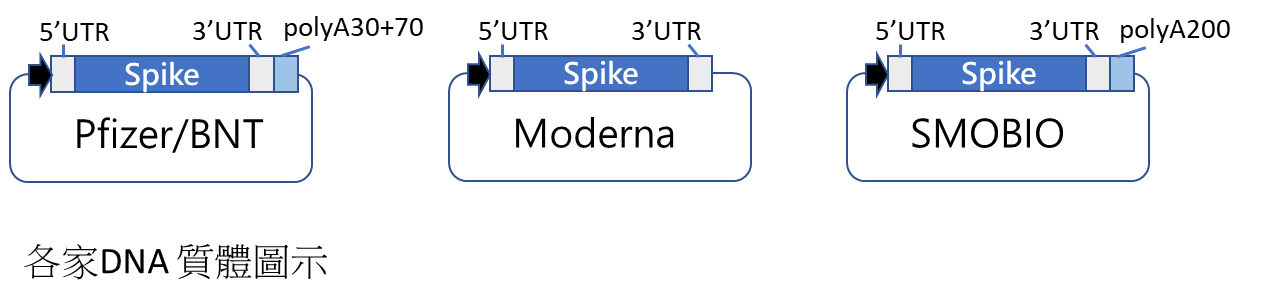
有些公司poly(A) tail的產生方式是另以 Poly(A) 聚合 酶於產生RNA後再行加上,故而於設計DNA質體的時候,就不需將poly(A) tail設計在質體中,兩種方式皆可採用。台灣新竹科學園區的鴻林堂生技(SMOBIO)在2021年建立了三種模板載體:1. Pfizer/BNT版本,自帶100個A鹼基、2. Moderna版本,無自帶A鹼基尾端,需進行聚合尾端的轉錄後修飾、3. SMOBIO自建版本,自帶200個A鹼基。